택란 추출물의 보충이 고지방식이 비만유도에 따른 산화스트레스와 간 기능에 미치는 영향
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Lycopus lucidus Turcz (LT), a perennial herb in the Lamiaceae family, has traditionally been used in East Asia for its anti-inflammatory and circulation-promoting effects and contains phenolic compounds with strong antioxidant activity. Despite this, in vivo studies verifying its efficacy are limited, and no research has directly compared extracts prepared with different solvents. This study compared the effects of LT water and ethanol extracts in HepG2 hepatocytes and evaluated the impact of LT water extract on oxidative stress, apoptosis, lipid metabolism, and liver function in diet-induced obese mice. In vitro, fatty acid-treated HepG2 cells exhibited marked lipid accumulation, which was reduced significantly by LT water and ethanol extracts without cytotoxic effects. In vivo, C57BL/6J mice were fed a normal diet (ND), high-fat diet (HFD), or HFD supplemented with low-dose (LLT) or high-dose (HLT) LT water extract for 12 weeks. LT supplementation reduced the levels of hepatic lipid droplets, plasma GOT and GPT, and inflammatory cytokines (IL-1β and TNF-α) elevated by the HFD. It also improved dyslipidemia and upregulated hepatic PPARα and PGC1α expression, promoting fatty acid oxidation. Furthermore, LT enhanced the antioxidant enzyme activities (SOD, CAT, GR, and GPx) and decreased caspase-3 and caspase-8 expression, alleviating hepatocellular apoptosis. These results suggest that LT supplementation improves the liver function by reducing oxidative stress, regulating lipid metabolism, and suppressing apoptosis, highlighting its potential as a functional food ingredient for preventing and managing non-alcoholic fatty liver disease (NAFLD). The beneficial effects appear to occur regardless of the extraction solvent (hot water or ethanol).
Keywords:
Lycopus lucidus Turcz Water Extract, high-fat diet, obesity, antioxidant property, hepatic steatosisⅠ. 서론
현대 사회에서 비만과 함께 비알콜성 지방간(non-alcoholic fatty liver disease, NAFLD)과 같은 간 질환은 전 세계적으로 증가하는 주요 건강 문제로, 대사 질환 및 심혈관계 질환의 주요 위험 요인이 되고 있다. 간은 포도당 신생합성 및 지질 대사 등 체내 에너지의 항상성 조절의 중심을 이루는 주된 장기로(Kim et al. 2021), 간 기능의 장애는 비만과 밀접한 상관관계가 있다. 비만은 말초 조직의 인슐린 저항성을 유발하며, 이는 지방 조직의 지질분해를 촉진시켜 혈중으로 유리지방산 분비를 증가시키며, 결과적으로 간 조직 내 이상 지질 축적을 초래해 지방간을 유발한다(Kuen et al. 2016). 비만으로 유도된 NAFLD는 비알코올성 지방간염(non-alcoholic steatohepatitis, NASH)과 간 섬유화를 거쳐 간경변증(liver cirrhosis)으로 진행될 수 있다. 그러나 현재 간경변증을 근본적으로 치료할 효과적인 약제가 없으므로, NAFLD 단계에서의 조기 관리가 매우 중요하다. 산화 스트레스(oxidative stress)는 지방간의 발생과 진행, 특히 지방 축적 단계에서부터 염증, NASH, 섬유화까지 연결되는 주요 병태 생리인자로 작용한다(Arroyave-Ospina et al. 2021). 따라서 간 내 지질대사를 조절하면서 항산화 활성을 갖는 소재 개발은 NAFLD 관리에 있어 필수적이다. 천연물 소재는 합성 약물에 비해 전반적으로 부작용 발생 위험이 낮고 장기간 섭취에도 안전성이 높은 경우가 많아 NAFLD 예방 및 치료를 위한 기능성 소재 개발에 유망한 자원으로 주목받고 있다.
‘쉽싸리’라고도 불리는 택란(LT, Lycopus lucidus Turcz)은 국화과(Asteraceae)에 속하는 여러해살이풀로, 한방에서는 그 뿌리를 ‘택란(澤闌)’이라 하여 약용으로 사용해 왔다. 택란의 주요 성분으로는 protocatechuic acid, caffeic acid, rutin, rosmarinic acid 등이 있으며, 대부분의 연구에서 rosmarinic acid를 주요 지표성분으로 설정하고 있다(Kim et al. 2018; Lee et al. 2019). 택란은 간 보호(Lee et al. 2019), 항산화(Ślusarczyk et al. 2009), 대사증후군 개선(Han et al. 2022) 등 다양한 효능이 보고되어 있으나, 택란 추출물의 효능을 검증한 in vivo 연구는 여전히 부족하며, 특히 추출 용매에 따른 효능 비교 연구는 보고된 바 없다. 이에 본 연구에서는 HepG2 간세포를 대상으로 택란 열수 추출물과 주정 추출물의 효능을 비교하고, 고지방식이로 유도된 비만 마우스를 이용하여 택란 열수 추출물이 산화스트레스, 세포사멸, 지질대사 조절을 통한 간 기능 개선에 미치는 영향을 규명하고자 하였다. 더 나아가, 본 연구는 택란 열수 추출물이 비알콜성 지방간질환(NAFLD)의 예방 및 관리용 기능성 소재로 활용될 수 있는 가능성을 제시하고자 한다.
Ⅱ. 연구방법
1. 실험재료
본 연구의 실험 재료는 Puremind(Yeongcheon, Korea)로부터 국내산 택란 건물을 구입하여 사용하였다. 수세 처리를 통해 흙과 먼지 등의 이물질을 제거하여 실온에서 24시간 이상 건조 후 5°C 이하에서 냉장 보관하면서 사용하였다.
2. 시료추출
건조시료 100 g을 각각 정밀히 달아 증류수 및 30% 에탄올 1 L를 넣은 후 60℃에서 3시간 추출을 3회 반복하였으며, 추출된 액을 여과하여 감압농축한 후 적당량 농축된 액을 동결시켜 동결건조 하였다. 수율은 열수추출물의 경우 27.36%, 에탄올추출물의 경우 28.52%이었다. 시료는 사용전까지 –70°C에 보관하였다.
3. 세포 배양 및 분화
인간 간암 세포주인 HepG2 세포는 10% FBS(Fetal Bovine Serum)과 1% penicillin-streptomycin을 함유한 Dulbecco’s Modified Eagle’s Medium(DMEM, gilbco, Grand Island, NY)에서 37℃, 5% CO₂ 조건에서 배양하였다. HepG2 세포의 confluency가 70~80%에 도달하면 6 well plate에 계대배양하였으며, 계대배양 2일째에 유리지방산(5mM)과 함께 택란 열수 및 주정추출물을 각 500 ㎍/mL 또는 1,000 ㎍/mL를 48시간 동안 처리하였다.
4. MTT(3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazolium Bromide) 측정
HepG2 세포를 96 well plate에 4×104 cells/well로 배양하고, 24시간 후에 각 well 당 택란 열수 및 주정추출물을 각 100, 250, 500, 750, 1,000, 1,500, 2,000 ㎍/mL 농도별로 처리하였다. 48시간 후, 각 well에 100 μgl MTT를 첨가하고 4시간 동안 반응시켰다. 배지를 제거한 뒤, 살아있는 세포 내에서 생성된 formazan 결정은 100 μL DMSO에 용해하였다. 세포 생존율은 SpectraMax i3 microplate reader(Molecular Devices, Sunnyvale, CA, USA)를 사용하여 570nm에서 측정하였다. 모든 처리는 3회 반복하여 수행하였다.
5. Oil Red O 염색
HepG2 세포를 10% formaldehyde 용액에 30분간 고정한 후, 실온에서 Oil Red O 용액으로 20분간 염색하였다. 이후 증류수로 세척한 뒤, 현미경(Olympus CKX 41)으로 염색된 세포를 관찰하고 이미지를 촬영하였다.
6. 실험동물
실험동물은 40마리의 4주령 C57BL/6J 웅성 마우스를 ㈜중앙실험동물(Seoul, Korea)에서 구입하여 1주일 동안 chow 식이로 적응시킨 후, 난괴법(randomized block design)에 따라 4군으로 나누어 12주간 실험을 진행하였다: (1) 정상식이(10 kcal% fat)를 급여한 ND군(Normal Diet); (2) 고지방식이(40 kcal% fat)을 급여한 HFD군(High-fat diet); (3) HFD를 급여하고 0.05% (w/w) LT 열수추출물을 식이보충한 LLT군(HFD + low dose of LT); (4) HFD를 급여하고 0.1% (w/w) LT 열수추출물을 식이보충한 HLT군(HFD + low dose of LT). 실험동물은 각각의 개별 cage 안에서 실험 식이와 식수를 자유롭게 섭취(ad libitum)하도록 하였으며, 사육실은 항온 22~24℃, 항습 45~55℃, 12시간 간격의 light cycle을 유지하였다. 동물실험은 경북대학교 동물실험윤리위원회의 승인(KNU 2023-0115)을 받아 진행하였다.
7. 해부 및 시료 수집
사육 종료 시점에 12시간 공복시킨 마우스를 isoflurane(5 mg/kg body weight, Baxter, USA) 흡입으로 마취한 후 개복하여 문맥(portal vein)에서 혈액을 채취하고 장기를 적출하였다. 채취한 혈액은 heparin으로 처리된 시험관에 즉시 수집한 뒤, 1,000×g, 4℃에서 15분간 원심분리하여 혈장을 수집하였다. 하층액은 0.9% 생리식염수로 2번 세척한 후 증류수와 1:1 비율로 혼합하여 용혈(hemolysis)을 유도하고, 적혈구를 수집하였다. 모든 시료는 분석 전까지 –70℃에 보관하였다.
8. 식이 섭취량, 체중 증가량 및 식이 효율 측정
체중과 식이섭취량은 실험 기간 12주 동안 매주 1회씩 측정하였으며, 식이 효율(food efficiency ratio: FER)은 일일 체중 증가량을 일일 에너지 섭취량으로 나눈 값을 사용하였다.
9. Dual-energy X-ray absortiometry (DXA) 측정
총 체지방율과 제지방율은 실험 종료 1주 전에 이중에너지 X선 흡수계측법(DXA; InAlyzer Dual X-ray Absorptiometry, Medikors, Seongnam, Korea)을 사용하여 측정하였다. 각 마우스의 체성분은 장비 소프트웨어를 이용해 분석하였으며, 체지방은 붉은색, 제지방은 파란색으로 표시하였다.
10. 혈장 생화학적 분석
혈장 중성지방, 총콜레스테롤 및 glutamic oxaloacetic transaminase(GOT)와 glutamic pyruvic transaminase(GPT) 활성도는 아산제약(Asan Pharm Co., Seoul, Korea)의 효소 kit를 사용하여 측정하였다. 혈장 유리지방산 측정은 효소법을 이용한 발색법 원리를 이용한 유리지방산 측정용 시액(Non-esterified fatty acid, NEFA kit, Wako, Osaka, Japan)을 사용하여 측정하였다. 혈장 cytokine(IL-1β and TNFα) 함량 측정은 Multiplex detection kit(Bio-rad, Hercules, CA, USA) 및 Luminex 200 labmap system (Bio-rad)를 사용하여 측정하였다.
11. 간 조직 형태학적 분석
조직의 형태학적 관찰을 위해 간 조직의 일부를 일정한 크기로 절단하여 10% formalin 용액(sigma-aldrich, St. Louis, Mo, USA)에 고정한 후, 알코올에 재고정하고 탈수 과정을 거쳐 파라민으로 포매하였다. 포매된 조직은 두께 4 μm로 절편을 제작하여 유리 슬라이드에 부착한 뒤 hematoxylin&eosin(H&E)(sigma-aldrich, St. Louis, Mo, USA)으로 염색하였다. 모든 염색된 샘플은 광학현미경(Nikon, Tokyo, Japan)으로 200배 배율로 관찰하였다.
12. 간 조직 지질 함량 분석
간 조직 지질은 Folch(1957)의 방법을 따라 추출하였다. 간 조직 0.1 g을 tissue lyzer를 이용해 분쇄한 후 2 mL phosphate buffer(pH 8.0) 용액으로 균질화시킨 후 chloroform:methanol(1:2) 용매로 추출하였다. 추출액을 37℃에서 질소가스로 휘발시켜 isopropanol(sigma-aldrich, St. Louis, Mo, USA)로 희석한 후, 정량을 위해 효소 시액에 유화제로 3 mM cholic acid(sodium salt)와 발색 시 일어나는 탁도(turbidity)를 제거하기 위하여 0.5% Triton X-100(sigma-aldrich, St. Louis, Mo, USA)을 혼합하여, 지질 성분을 추출한 후 혈장 중성지질 및 콜레스테롤 정량법과 동일하게 정량하였다.
13. 적혈구 항산화 효소 활성도 분석
적혈구 superoxide dismutase(SOD)는 superoxide anion radical (O2-)을 H2O2 및 O2로 분해하는 반응을 촉매하는 효소로서 활성도 측정은 Marklund(1974)의 방법을 이용하여 알칼리 상태에서 pyrogallol의 자동산화에 의한 발색 정도를 이용하여 측정하였다. Catalase(CAT)는 H2O2를 H2O 및 O2로 분해하는 역할을 하며 활성도 측정은 Abei(1974)의 방법으로 측정하였다. Glutathione reductase(GR) 활성도는 산화형 glutathione(GSSG)가 NADPH 및 GR의 작용으로 환원형 glutathione(GSH)으로 전환될 때 NADPH가 감소하는 정도를 Pinto(1969)의 방법을 이용하여 측정하였다. Glutathione peroxidase(GSH-Px) 활성도는 Paglia와 Valentine(1967)의 방법을 이용하여 측정하였다.
14. 정량적 실시간 PCR(Quantitative real-time PCR, RT-qPCR) 분석
HepG2 세포 및 동물실험의 간 조직에서 총 RNA는 TRIzol을 사용하여 분리하였다. 총 RNA (1 µg)로부터 cDNA는 reverse transcription kit (Elpisbio Inc., Daejeon, Korea)를 이용하여 합성하였다. RT-qPCR은 RNase-free water (Enzynomics Co., Daejeon, Korea)로 희석한 cDNA, SYBR Green(Enzynomics Co.) 및 프라이머(Genotech Co., Daejeon, Korea)를 사용하여 수행하였다(Table 1). 데이터 분석은 CFX Duet 시스템을 사용하였으며, CT 값은 GAPDH로 정규화하였다.
15. Western blot을 이용한 단백질 발현 수준 분석
간 조직 단백질은 Pierce BCA protein assay kit(Thermo Scientific, USA)를 사용하여 정량하였다. 단백질 시료는 10% SDS-폴리아크릴아마이드 겔에 전기영동한 뒤 PVDF 멤브레인으로 전이하였다. 이후 5% 탈지분유(TBS에 0.1% Tween-20 포함)로 실온에서 1시간 동안 블로킹하였다. TBS-T로 세척한 후, 멤브레인을 1차 항체와 함께 4°C에서 하룻밤 동안 반응시켰다. 다시 TBS-T로 세척한 뒤, 2차 항체와 실온에서 반응시켰다. 항체의 상세 정보는 Table 2에 제시하였다. 단백질 밴드는 WESTAR ETA C ULTRA 2.0(XLS075,0100, Cyanagen)을 사용하여 검출하였으며, Fusion evo-6 series 및 소프트웨어(Vilber Lourmat, France)를 이용해 시각화하였다.
16. 통계처리
본 실험을 통해 얻어진 결과는 SPSS(Statistical Package for the Social Sciences ver 23.0, SPSS Institute Inc., Chicago, IL, USA)를 이용하여 통계 분석하였다. 모든 결과는 mean ± S.E.(standard error)로 나타내었으며, ND군과 HFD군간의 유의성 검정을 위해 Student’s t-test를 실시하고, 고지방식이 군 간의 유의성 검정은 분산분석(ANOVA)을 한 후 p<0.05 수준에서 Duncan’s multiple range test에 의해 검정하였다.
Ⅲ. 결과 및 고찰
1. HepG2 세포에서 택란 추출 용매의 효능비교
HepG2 세포에서 택란(LT)의 열수추출물 및 에탄올 추출물의 세포독성을 평가하였다(Fig. 1A). 택란의 열수추출물 및 에탄올추출물 모두 2,000 ㎍/ml의 고농도에서도 세포독성을 나타내지 않았다.
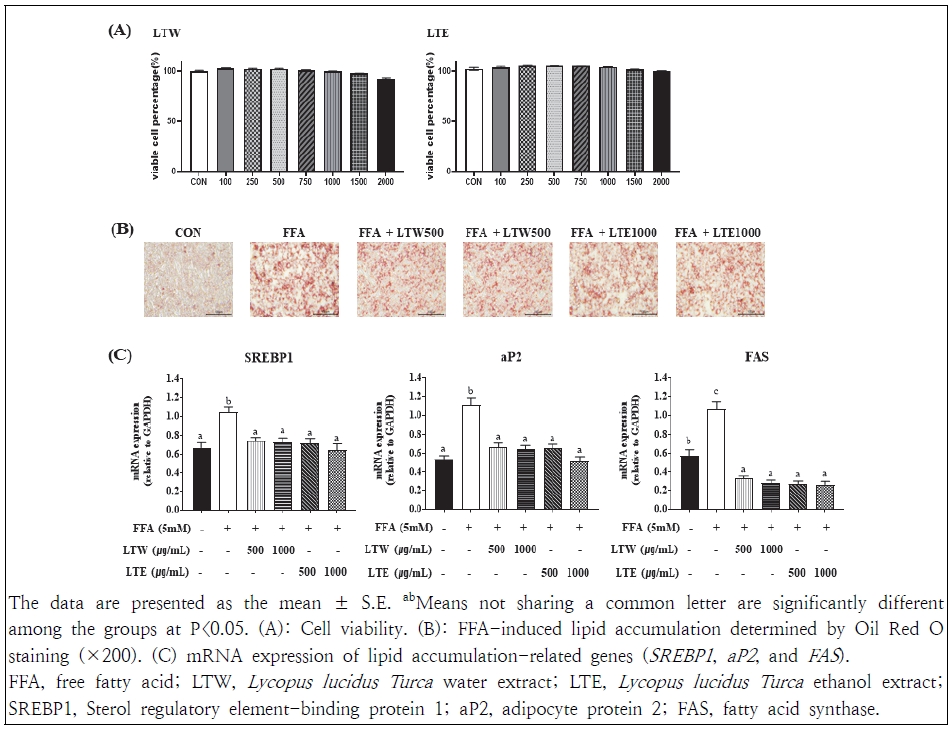
Effects of Lycopus lucidus Turcz on cell viability, lipid accumulation, and lipogenesis-related gene expression in HepG2 cells.
택란의 지질 축적 억제 효과를 확인하기 위해 HepG2 세포에서 5 mM 지방산을 처리한 후 택란 열수추출물 및 에탄올추출물 각각 500, 1,000 ㎍/ml 농도로 처리하고, 세포 내 지질함량을 Oil Red O 염색을 통해 평가하였다(Fig. 1B). 현미경 관찰 결과 지방산 처리군의 HepG2 세포는 무처리 대조군과 달리 심한 지방증이 관찰되었다. 반면, 택란 열수추출물 및 에탄올추출물 처리군에서는 지질 축적이 유의적으로 감소하였으며, 1,000 ㎍/ml 농도에서 뿐만 아니라 더 낮은 농도인 500㎍/ml에서도 지질 축적이 현저하게 감소하였다.
택란의 지방간 개선 효능을 규명하기 위해 지방산을 처리한 HepG2 세포에서 간 지방합성의 핵심 바이오마커인 SREBP1, aP2, FAS의 발현을 RT-qPCR로 분석하였다(Fig. 1C). SREBP1은 간에서 새로운 지방산 합성(de novo lipogenesis, DNL)을 조절하는 핵심 전사인자로, 고지방 식이 등 대사적 자극에 의해 활성화된다(Moon et al. 2012). 분석 결과, 택란 추출물은 추출 용매(열수 또는 주정)와 관계없이 SREBP1 발현을 현저히 억제하였다. 또한 SREBP1의 하위 표적 단백질로 알려진 aP2와 FAS의 발현 역시 지방산으로 유도된 HepG2 세포에서 택란 추출물 처리에 의해 유의적으로 감소하였다. aP2는 세포 내 지방산과 장쇄지방산의 결합 및 운반을 담당하는 세포질 단백질로, 과발현 시 간 세포 내 지방 축적과 염증을 악화시키는 것으로 알려져 있다(Furuhashi et al. 2015). FAS는 지방산 합성의 핵심 효소로, 고지방ㆍ고탄수화물 식이에 의해 발현이 증가하며 간 내 지방산 합성을 촉진한다(Gao et al. 2023). 종합적으로, 택란 추출물은 추출 용매와 무관하게 500 ㎍/ml 이상의 농도에서 SREBP1, aP2, FAS 등 지질 합성 관련 유전자의 발현을 조절함으로써 지방산으로 유도된 HepG2 세포의 지방간을 개선할 수 있음을 시사한다. 또한 기능성 식품 소재로서의 활용 가능성을 고려할 때, 제조 비용이 높은 주정 대신 열수 추출 조건만으로도 지방간 개선 효과를 발휘할 수 있음을 보여준다.
2. 체중, 식이 섭취량, 식이효율 및 체성분 변화
세포실험 결과, 지방간 개선 효과에 있어 택란(LT) 열수추출물과 주정추출물 간 유의한 차이가 없음을 확인하였으며, 산업화 가능성을 고려하여 동물실험에서는 택란 열수추출물의 농도별 효능을 평가하였다. 실험군은 정상식이군(ND), 고지방식이군(HFD), 고지방식이+저농도 택란 열수추출물 보충군(LLT), 고지방식이+고농도 택란 열수추출물 보충군(HLT)으로 나누어 12주간 사육하였다. 체중 변화, 식이 섭취량 및 식이효율 분석 결과는 Table 3에 제시하였다. HFD군은 ND군에 비해 최종 체중, 일일 체중 증가량, 일일 에너지 섭취량 및 식이효율이 모두 유의하게 증가하여 고지방식이에 의한 비만 유도가 성공적으로 이루어졌음을 확인하였다. 반면, LT 보충군인 LLT군과 HLT군은 최종 체중과 일일 체중 증가량이 HFD군에 비해 유의하게 감소하여, 농도와 관계없이 비만이 효과적으로 개선됨을 확인하였다. 일일 에너지 섭취량은 LLT군과 HLT군 모두 HFD군보다 유의하게 낮았으나, 식이효율은 HFD군과 통계적으로 유의한 차이가 없었다. 따라서 택란 보충에 의한 체중 감소는 에너지 섭취량 감소와 밀접한 관련이 있는 것으로 판단된다.

Effects of Lycopus lucidus Turcz for 12 weeks on body weight gain, food intake, and FER in HFD-induced obese mice.
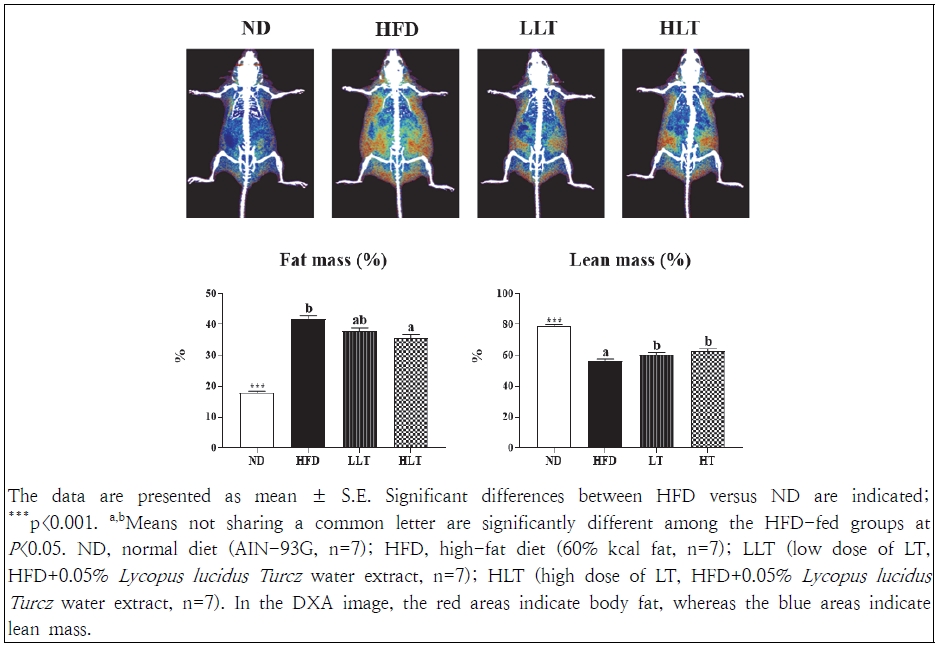
DXA를 이용한 체성분 분석 결과는 Fig. 2에 제시하였다. HFD군의 체지방률은 ND군에 비해 유의하게 증가한(p<0.001) 반면, 제지방률은 감소하여 체중 증가와 함께 체지방률이 상승했음을 확인하였다. 택란 열수추출물 보충군은 농도 의존적으로 체지방률을 감소시켰으며, 제지방률은 농도와 관계없이 HFD군에 비해 유의하게 증가시켰다(p<0.05). 이러한 결과는 택란 열수추출물 보충이 고지방식이로 유도된 비만에 따른 체지방 증가 및 제지방 감소를 개선하는 데 효과적일 가능성을 시사한다.
3. 혈장 생화학적 분석
택란 열수추출물 보충에 따른 혈장 유리지방산, 중성지질, 콜레스테롤 농도 변화는 Table 4에 제시하였다. 고지방식이군(HFD)은 정상식이군(ND)에 비해 혈장 유리지방산(p<0.01), 중성지질(TG) (p<0.001), 콜레스테롤(p<0.001) 농도가 유의하게 증가하여 이상지질혈증이 유도되었다. 고지방식이에 의한 비만 상태에서는 인슐린 저항성이 동반되며, 이는 지방조직의 지방분해를 촉진해 혈장 유리지방산 농도를 높이고, 결과적으로 간 내 과도한 지질 축적을 초래하여 지방간을 유발한다(Kuen et al. 2016). 또한 간 내 중성지질의 과도 축적은 VLDL 대사 장애를 유발하여 혈장 중성지질 및 콜레스테롤 농도 증가에 기여한다. 따라서 고지방식이에 의해 지방간이 진행될수록 혈중 유리지방산, 중성지질, 콜레스테롤 농도는 함께 상승한다(Heeren & Scheja 2021). 한편, 고지방식이로 증가한 혈장 유리지방산, 중성지질, 콜레스테롤 농도는 택란 열수추출물 보충군(LLT, HLT)에서 모두 유의하게 감소하였으며, 이는 택란 열수추출물이 지방간 개선에 효과적일 가능성을 시사한다.

Effects of Lycopus lucidus Turcz for 12 weeks on the plasma lipid and cytokine levels in HFD-induced obese mice
염증성 사이토카인인 IL-1β와 TNF-α는 산화 스트레스와 지질 과산화를 유발하여 간세포 손상, 염증, 섬유화를 촉진한다(Day & James 1998). 특히 이들 사이토카인의 혈중 수준은 비만 및 대사 스트레스 상황에서 증가하며, 인슐린 저항성 및 NAFLD와 높은 상관을 보인다(Vachliotis & Polyzos 2023). 본 연구에서 택란 열수추출물은 저농도와 고농도 모두에서 고지방식이에 의해 상승한 혈장 IL-1β와 TNF-α 농도를 유의하게 감소시켜(p<0.05), 고지방식이 유발 염증-대사 이상 개선에 기여할 가능성을 시사한다.
4. 간 조직 중량, 조직학적 관찰, 간 조직 지질, 혈장 GOT, GPT 및 간 조직 단백질 발현 분석
간 조직은 지질대사 항상성을 유지하는 핵심 장기로, 고지방식이와 인슐린 저항성 등 대사 스트레스 상황에서는 간 내 지방산 유입 증가, SREBP-1 경로 활성화에 따른 신생 지방산 합성 증가, VLDL 분비 장애가 동시에 발생한다. 이로 인해 중성지질과 콜레스테롤이 간세포 내 과도하게 축적되면서 간 조직이 비대해지고, 비알코올성 지방간질환(NAFLD)이 유발된다(Kwon et al. 2018). 12주간 고지방식이로 비만을 유도한 마우스의 간 조직 중량 변화는 Fig. 3A에 제시하였다. 고지방식이군은 정상식이군에 비해 간 조직 중량이 유의적으로 증가하였으나, 택란 열수추출물 보충군은 HFD군 대비 간 조직 중량이 유의하게 감소하였다(p<0.05).
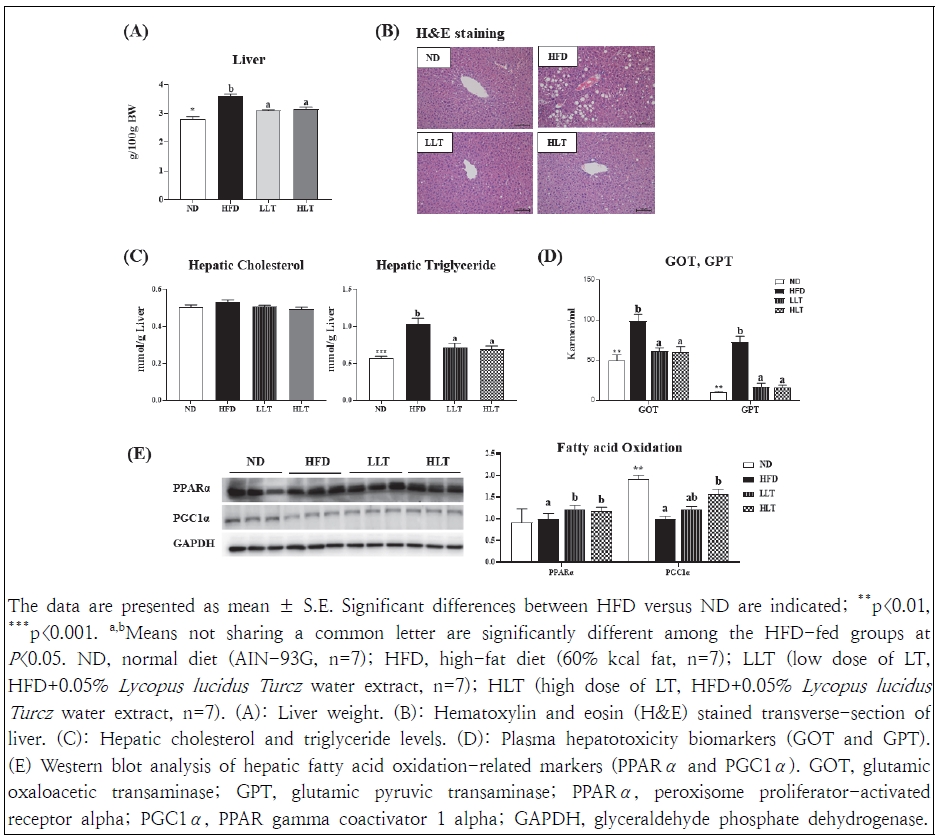
Effects of Lycopus lucidus Turcz for 12 weeks on the liver weight, morphology, hepatic lipid and hepatotoxicity marker levels, and fatty acid oxidation-related protein expression in HFD-induced obese mice.
H&E 염색 결과, 정상식이군은 간문맥을 중심으로 지방구가 없는 정상적인 간 조직 구조를 보였으나, 고지방식이군에서는 간 조직 중량 증가와 함께 간문맥 주변에 크고 작은 다수의 지방구가 축적되어 있었다(Fig. 3B). 이러한 지방구 축적은 택란 열수추출물 보충에 의해 현저히 감소하였다. 간 조직 내 콜레스테롤과 함량은 고지방식이군과 정상식이군과의 유의적인 차이가 관찰되지 않았으나, 중성지방 함량은 고지방식이군에서 정상식이군보다 유의하게 증가하였으며(p<0.001), 택란 열수추출물 보충 시 중성지방 함량이 유의하게 감소하였다(p<0.05)(Fig. 3C). 종합적으로, 택란 열수추출물은 간 조직 내 중성지질 함량을 감소시켜 지방구 축적을 억제하고, 이러한 효과는 간 조직 중량 감소와 밀접하게 관련된 것으로 판단된다.
GOT와 GPT는 간세포에 풍부하게 존재하는 효소로, 고지방식이, 과잉 칼로리 섭취, 인슐린 저항성 등에 의해 간세포 내 중성지방이 과도하게 축적되면 지질독성(lipotoxicity), 산화 스트레스, 염증 반응이 유발된다. 이로 인해 간세포막 손상 또는 세포사멸이 일어나면서 세포질 내 GOT와 GPT가 혈중으로 방출되어 수치가 상승하며, 간 손상의 지표로 활용된다(Reitman et al. 1957; Kwon et al. 2015). 본 연구에서 혈장 GOT 및 GPT 농도를 측정한 결과(Fig. 3D), 고지방식이군은 정상식이군에 비해 두 효소 모두 유의하게 상승하였으나, 택란 열수추출물 보충군에서는 현저한 감소가 관찰되었다.
NAFLD는 신생 지방산 합성 증가, VLDL 분비 장애뿐만 아니라 지방산 산화 감소에 의해서도 유발된다. PPARα는 지방산의 β-산화 경로를 전사 수준에서 활성화하는 핵심 전사인자로, 간 내 과잉 지방을 연소하는 스위치 역할을 한다(Pawlak et al. 2015). PGC-1α는 PPARα의 공활성인자로 작동하여 미토콘드리아 생합성과 지방산 산화를 동시에 촉진한다(Puigserver & Spiegelman 2003). 따라서 PPARα/PGC-1α 축을 함께 활성화하면 간 내 중성지질과 염증 수준을 낮추고, 미토콘드리아 기능을 강화하여 지방간 대사 개선을 가속화할 수 있다. 본 연구에서 간 조직 내 PPARα와 PGC1α의 단백질 발현을 western blot으로 분석한 결과(Fig. 3E), 고지방식이군의 경우 PGC-1α 단백질 발현이 현저히 감소하였으나, PPARα 단백질 발현에는 유의한 변화가 없었다. 반면, 택란 열수추출물 보충군에서는 농도와 관계없이 PPARα 단백질 발현이 HFD군보다 유의하게 증가하였으며(p<0.05), PGC-1α 단백질 발현은 농도 의존적으로 증가하였다. 이러한 결과는 택란 열수추출물이 PPARα/PGC-1α 축을 활성화시켜 NAFLD 개선에 기여할 수 있음을 시사한다.
5. 항산화활성 및 간 세포 사멸
NAFLD 진행의 핵심 유발 인자는 산화스트레스(ROS)와 지질과산화이다. 과도한 지방산 유입, DNL 증가, 미토콘드리아 기능 저하로 ROS가 상승하고, 이는 염증ㆍ세포 손상ㆍ섬유화를 가속화하여 단순 지방증에서 NASH로의 진행을 촉진한다(Angelico et al. 2024). 본 연구에서 택란 열수추출물의 항산화능을 평가하기 위해 superoxide dismutase(SOD), catalase(CAT), glutathione reductase(GR), glutathione peroxidase(GPx) 효소 활성을 분석한 결과는 Fig. 4A에 제시하였다. 고지방식이는 전반적으로 적혈구 항산화 효소 활성을 저하시키는 반면, 택란 열수추출물 보충은 SOD, CAT, GR, GPx 활성을 모두 유의하게 증가시켰으며(p<0.05), 특히 GR과 GPx 활성은 농도 의존적으로 증가하였다. 따라서 택란 열수추출물은 적혈구 항산화 효소 활성을 증강함으로써 우수한 항산화능을 나타내며, 이는 간 조직 내 지질 수준 감소와 혈중 염증 지표 개선에 기여하는 것으로 판단된다.
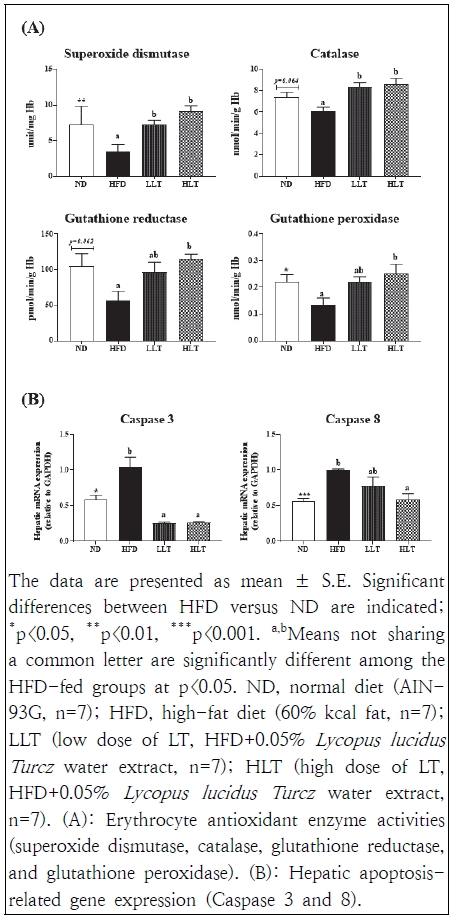
Effects of Lycopus lucidus Turcz for 12 weeks on the antioxidant activities and hepatic apoptosis-related gene expression in HFD-induced obese mice.
NAFLD의 병태생리에서 산화스트레스 증가는 지질과산화와 염증을 유발하여 간세포 apoptosis를 촉진하고, 이 과정에서 caspase-8이 상위 개시인자, caspase-3가 실행인자로 작동한다(Chen et al. 2020). 항산화 방어가 불충분할수록 이러한 사멸 신호가 강화되어 단순 지방증에서 NASH 및 섬유화로의 진행 위험이 커지며, SOD 축의 강화는 세포사멸을 완화하여 NAFLD를 개선하는 것으로 보고된다(Kumar et al. 2013). 본 연구에서 택란 열수추출물 보충은 고지방식이에 의해 증가한 간 조직의 caspase-3 및 caspase-8 유전자 발현을 유의적으로 감소시켜, 세포사멸의 개시와 실행 단계를 억제함으로써 지방간 개선에 기여하는 것으로 제시된다(Fig. 4B). 또한 이러한 효능은 택란 열수추출물에 의해 증가된 항산화능과 관련될 수 있음을 시사한다.
Ⅳ. 요약 및 결론
비알코올성 지방간(NAFLD)은 국내 성인의 절반가량이 발병 위험군에 속하는 대사성 간질환으로, 고지방식이와 비만은 주요 원인으로 알려져 있다. 본 연구에서는 고지방식이로 비만 및 지방간을 유도한 마우스 모델을 이용하여, 택란(Lycopus lucidus Turcz) 열수추출물이 체중, 지방간, 지질대사, 염증 및 항산화 반응에 미치는 영향을 종합적으로 분석하였다. 세포 수준에서 택란 열수추출물과 주정추출물은 고농도에서도 세포 독성이 관찰되지 않았으며, 지방산 처리로 유도된 HepG2 세포의 중성지질 축적을 억제하였다. 또한, 지방 합성 경로의 핵심 조절 전사인자인 SREBP1 및 그 하위 표적 유전자(aP2, FAS)의 발현을 낮추어, 추출 용매와 관계없이 지질 합성 억제 효과를 나타냈다. 산업적 활용성을 고려할 때, 열수추출만으로도 주정추출물과 유사한 개선 효과를 확인하였다. 동물실험에서는 택란 열수추출물 보충군이 고지방식이군 대비 최종 체중과 체지방률을 낮추고 제지방률을 증가시켰다. 혈중 유리지방산, 중성지질, 총콜레스테롤 농도와 염증성 사이토카인(IL-1β, TNF-α) 수치가 모두 감소하였으며, 이는 전신 대사 염증 반응이 완화된 결과로 해석된다. 간 조직 분석 결과, 택란 열수추출물은 간 중성지질 함량과 지방구 축적을 줄였으며, 혈중 GOT와 GPT 수치를 낮추어 간 손상 완화에 기여하였다. 더불어, 지방산 산화 경로의 핵심 인자인 PPARα 발현을 증가시키고, 그 공활성인자인 PGC-1α 발현을 농도 의존적으로 높여 미토콘드리아 기능 향상과 지질대사 활성화를 촉진하였다. 항산화 효소 활성 분석에서 SOD, CAT, GR, GPx가 전반적으로 증가하였으며, 특히 GR과 GPx의 활성은 택란 열수추출물 농도에 비례하여 상승하였다. 이러한 항산화능 강화는 간 조직에서 caspase-3 및 caspase-8 발현을 억제하여 세포사멸 신호를 차단하는 데 기여한 것으로 보인다. 결론적으로, 택란 열수추출물은 지질합성 억제, 지방산 산화 촉진, 항산화 방어 강화, 염증 완화, 세포사멸 억제를 통해 고지방식이로 유발된 비만 및 NAFLD를 개선하는 복합적인 작용을 나타냈다. 이러한 다중 기전 기반의 효과는 택란 열수추출물이 향후 NAFLD 예방ㆍ관리용 기능성 소재로 활용될 잠재력을 뒷받침한다.
Acknowledgments
This research was supported by Kyungpook National University Development Project Research Fund, 2022
References
-
Aebi H(1974) Catalase. In: Bergmeyer HV, ed. Methods in Enzymatic Analysis. New York: Academic Press, pp673-684
[https://doi.org/10.1016/B978-0-12-091302-2.50032-3]

-
Angelico F, Alcantara-Payawal D, Abdul Rani R, Mustafa N, Thongtang N, Chaiteerakij R, Bunchorntavakul C, Sukonthasarn A(2024) Review and expert opinion on MAFLD, oxidative stress and multifunctional management. Drugs Context 13, 2023-9-3.
[https://doi.org/10.7573/dic.2023-9-3]

-
Arroyave-Ospina JC, Wu Z, Geng Y, Moshage H(2021) Role of oxidative stress in the pathogenesis of non-alcoholic fatty liver disease: implications for prevention and therapy. Antioxidants 10(2), 174.
[https://doi.org/10.3390/antiox10020174]

-
Chen Z, Tian R, She Z, Cai J, Li H(2020) Role of oxidative stress in the pathogenesis of nonalcoholic fatty liver disease. Free Radic Biol Med 152, 116-141.
[https://doi.org/10.1016/j.freeradbiomed.2020.02.025]

-
Day CP, James OF(1998) Steatohepatitis: a tale of two “hits”? Gastroenterology 114(4), 842-845.
[https://doi.org/10.1016/S0016-5085(98)70599-2]

-
Folch J, Lees M, Sloane Stanley GH(1957) A simple method for the isolation and purification of total lipides from animal tissues. J Biol Chem 226(1), 497-509
[https://doi.org/10.1016/S0021-9258(18)64849-5]

-
Furuhashi M, Saitoh S, Shimamoto K, Miura T(2015) Fatty acid-binding protein 4 (FABP4): pathophysiological insights and potent clinical biomarker of metabolic and cardiovascular diseases. Clin Med Insights Cardiol 8(Suppl 3), 23-33.
[https://doi.org/10.4137/CMC.S17067]

-
Gao R, Li Y, Xu Z, Zhang F, Xu J, Hu Y, et al.(2023) Mitochondrial pyruvate carrier 1 regulates fatty acid synthase lactylation and mediates treatment of nonalcoholic fatty liver disease. Hepatology 78(6), 1800-1815.
[https://doi.org/10.1097/HEP.0000000000000279]

-
Han Y, Choi JY, Kwon EY(2022) Lycopus lucidus Turcz water extract ameliorates the metabolic disorder by up-regulated major urinary protein expression in high-fat diet-induced obesity. Curr Issues Mol Biol 44(5), 2417-2430.
[https://doi.org/10.3390/cimb44050165]

-
Heeren J, Scheja L(2021) Metabolic-associated fatty liver disease and lipoprotein metabolism. Mol Metab 50, 101238.
[https://doi.org/10.1016/j.molmet.2021.101238]

-
Kim KY, Oh TW, Ma JY, Park KI(2018) Ethanol extract of Lycopus lucidus Turcz ex Benth inhibits metastasis by downregulation of Runx-2 in mouse colon cancer cells. Evid Based Complement Alternat Med 2018, 9513290.
[https://doi.org/10.1155/2018/9513290]

-
Kim TH, Hong DG, Yang YM(2021) Hepatokines and non-alcoholic fatty liver disease: linking liver pathophysiology to metabolism. Biomedicines 9(12), 1903.
[https://doi.org/10.3390/biomedicines9121903]

-
Kumar A, Sharma A, Duseja A, Das A, Dhiman RK, Chawla YK, Kohli KK, Bhansali A(2013) Patients with nonalcoholic fatty liver disease (NAFLD) have higher oxidative stress in comparison to chronic viral hepatitis. J Clin Exp Hepatol 3(1), 12-18.
[https://doi.org/10.1016/j.jceh.2012.10.009]

-
Kwon EY, Jung UJ, Park T, Yun JW, Choi MS(2015) Luteolin attenuates hepatic steatosis and insulin resistance through the interplay between the liver and adipose tissue in mice with diet-induced obesity. Diabetes 64(5), 1658-1669.
[https://doi.org/10.2337/db14-0631]

-
Kwon EY, Shin SK, Choi MS(2018) Ursolic acid attenuates hepatic steatosis, fibrosis, and insulin resistance by modulating the circadian rhythm pathway in diet-induced obese mice. Nutr 10(11), 1719.
[https://doi.org/10.3390/nu10111719]

-
Lee MR, Yang HJ, Park KI, Ma JY(2019) Lycopus lucidus Turcz ex Benth attenuates free fatty acid-induced steatosis in HepG2 cells and non-alcoholic fatty liver disease in high-fat diet-induced obese mice. Phytomedicine 55, 14-22.
[https://doi.org/10.1016/j.phymed.2018.07.008]

-
Marklund S, Marklund G(1974) Involvement of the superoxide anion radical in the autoxidation of pyrogallol and a convenient assay for superoxide dismutase. Eur J Biochem 47(3), 469-474.
[https://doi.org/10.1111/j.1432-1033.1974.tb03714.x]

-
Moon YA, Liang G, Xie X, Frank-Kamenetsky M, Fitzgerald K, Koteliansky V, Brown MS, Goldstein JL, Horton JD(2012) The Scap/SREBP pathway is essential for developing diabetic fatty liver and carbohydrate-induced hypertriglyceridemia in animals. Cell Metab 15(2), 240-246.
[https://doi.org/10.1016/j.cmet.2011.12.017]

- Paglia DE, Valentine WN(1967) Studies on the quantitative and qualitative characterization of erythrocyte glutathione peroxidase. J Lab Clin Med 70(1), 158-169
-
Pawlak M, Lefebvre P, Staels B(2015) Molecular mechanism of PPARα action and its impact on lipid metabolism, inflammation and fibrosis in non-alcoholic fatty liver disease. J Hepatol 62(3), 720-733.
[https://doi.org/10.1016/j.jhep.2014.10.039]

-
Pinto RE, Bartley W(1969) The effect of age and sex on glutathione reductase and glutathione peroxidase activities and on aerobic glutathione oxidation in rat liver homogenates. Biochem J 112(1), 109-115.
[https://doi.org/10.1042/bj1120109]

-
Puigserver P, Spiegelman BM(2003) Peroxisome proliferator-activated receptor-γ coactivator 1α (PGC-1α): transcriptional coactivator and metabolic regulator. Endocr Rev 24(1), 78-90.
[https://doi.org/10.1210/er.2002-0012]

-
Reitman S, Frankel S(1957) A colorimetric method for the determination of serum glutamic oxalacetic and glutamic pyruvic transaminases. Am J Clin Pathol 28(1), 56-63.
[https://doi.org/10.1093/ajcp/28.1.56]

-
Ślusarczyk S, Hajnos M, Skalicka-Woźniak K, Matkowski A(2009) Antioxidant activity of polyphenols from Lycopus lucidus Turcz. Food Chem 113(1), 134-138.
[https://doi.org/10.1016/j.foodchem.2008.07.037]

-
Vachliotis ID, Polyzos SA(2023) The role of tumor necrosis factor-alpha in the pathogenesis and treatment of nonalcoholic fatty liver disease. Curr Obes Rep 12(3), 191-206.
[https://doi.org/10.1007/s13679-023-00519-y]

-
Yang KC, Hung HF, Lu CW, Chang HH, Lee LT, Huang KC(2016) Association of Non-alcoholic Fatty Liver Disease with Metabolic Syndrome Independently of Central Obesity and Insulin Resistance. Sci Rep 6, 27034.
[https://doi.org/10.1038/srep27034]