감귤껍질 분말 첨가가 쌀 모닝빵의 항산화 활성 및 페놀 화합물 조성에 미치는 영향
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
This study investigated how the incorporation of citrus (Citrus unshiu Marcov.) peel powder (0, 3, 6, and 9 % w/w) influences the antioxidant capacity and phenolic profile of rice morning bread. Powder addition significantly increased the total phenolic, flavonoid, and carotenoid contents; 9 % supplementation resulted in a 3.7-fold increase in the total phenolic content compared to the control. The antioxidant activities measured by DPPH (2,2-diphenyl-1-picrylhydrazyl), ABTS (2,2′-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid)), and FRAP (ferric ion reducing antioxidant potential) assays increased accordingly and were strongly correlated with the total phenolics (r ≥ 0.98, p < 0.05). High-performance liquid chromatography with diode-array detection analysis quantified 15 phenolic acids and two flavonols. The levels of gallic, vanillic, syringic, chlorogenic, and trans-ferulic acids, together with rutin and quercetin, increased markedly as supplementation rose. These results suggest that citrus peel powder can serve as an effective clean-label ingredient for enhancing the bioactive compound content of rice-based bakery products, while also offering a sustainable and value-added use for citrus processing by-products.
Keywords:
citrus peel powder, rice morning bread, antioxidant activity, phenolic acids, functional bakeryⅠ. 서론
쌀은 우리나라의 주식으로서 오랜 기간 식생활의 중심을 차지해왔으나, 1인 가구의 증가, 외식ㆍ간편식 선호, 식생활의 서구화 등으로 인해 1인당 쌀 소비량은 지난 30여 년간 절반 이하로 감소하였다(Rural Development Administration 2022). 이에 따라 농업 및 식품산업계에서는 쌀의 소비를 확대하기 위한 다양한 대체 활용 방안이 요구되고 있으며, 특히 밀가루를 대체할 수 있는 글루텐 프리(gluten-free) 소재로서 쌀가루의 기능성과 응용 가능성이 주목받고 있다. 최근 연구에 따르면 쌀가루는 부드러운 질감과 소화가 용이한 특성을 지녀, 특히 고령자ㆍ유아ㆍ소화기 질환자 등 특정 소비층뿐 아니라 건강 지향 소비자들로부터 긍정적 반응을 얻고 있는 것으로 보고되고 있다(Cornejo & Rosell 2015; Lee 2015; Bourekoua et al. 2016).
실제 쌀가루를 활용한 베이커리 제품은 밀가루 대비 글루텐 불내성 문제를 해소할 수 있을 뿐 아니라, 지방 함량이 낮고 단백질 품질이 우수하다는 장점을 갖는다(Song & Shin 2007). 특히 쌀 모닝빵은 반죽의 점탄성, 구움 후 내부 조직감, 부드러움 등이 소비자의 기호에 직접 영향을 미치는 대표적 모델 식품으로, 글루텐 대체 기능성을 평가하는 지표로 널리 활용되고 있다(Cornejo & Rosell 2015; Park & Kim 2023).
최근 베이커리 시장은 단순한 열량 공급을 넘어서 기능성과 건강 기여도를 중시하는 방향으로 전환되고 있으며, 이에 따라 항산화, 항염, 혈당조절, 체중관리 등의 생리활성을 갖는 소재의 개발과 적용이 활발히 이루어지고 있다(Shahidi & Ambigaipalan 2015). 특히 과일 껍질, 채소 분말, 곡류 부산물 등 식물성 천연 기능성 소재를 베이커리 반죽에 첨가하는 연구가 지속적으로 보고되고 있으며, 이들 소재는 폴리페놀류, 플라보노이드, 카로티노이드 등 다양한 항산화 성분을 포함하고 있어 제품의 품질과 기능성 향상에 기여할 수 있다(Manach et al. 2004; Sedej et al. 2011).
한편 국내 감귤 가공 산업에서는 연간 약 60,000 톤 이상의 감귤 껍질 부산물이 발생하며, 현재 대부분이 매립, 사료 또는 비료로 단순 활용되고 있다(Lee et al. 2024). 그러나 최근 연구에 따르면 감귤껍질은 식이섬유, 비타민 C, 플라보노이드(hesperidin, narirutin, naringin), 그리고 chlorogenic acid, ferulic acid, gallic acid 등 다양한 페놀산류를 고농도로 함유하고 있어 식품 기능성 소재로서 활용 가능성이 매우 높다(Manthey & Grohmann 2001; Li et al. 2006; González-Molina et al. 2010). 이러한 생리활성 화합물은 강력한 항산화, 항염, 혈중 지질 개선 효과를 나타내며, 체내 산화스트레스 조절과 만성질환 예방에도 기여하는 것으로 알려져 있다(Rice-Evans et al. 1997; Rao & Rao 2007).
Lee et al.(2016)은 감귤껍질 분말을 3–9% 수준으로 첨가한 밀 모닝빵을 인체에 적용한 연구에서 혈중 총콜레스테롤 및 체지방률 감소에 긍정적 효과를 보고하였지만, 제품 내 기능성 성분의 정량적 변화나 항산화 활성 지표에 대한 구체적인 분석은 이루어지지 않았다. 따라서 감귤껍질의 함량에 따른 제품 내 항산화 성분 조성과 생리활성 지표의 변동을 과학적으로 규명하는 추가적인 연구가 요구된다.
이에 본 연구는 쌀가루를 주원료로 하여 글루텐 프리 베이커리 제품인 모닝빵을 제조하고, 여기에 감귤껍질 분말을 0, 3, 6, 9% 첨가하여 총 페놀 함량, 총 플라보노이드 함량, 총 카로티노이드 함량, 그리고 DPPH, ABTS, FRAP를 이용한 항산화 활성을 평가하고자 하였다. 또한, HPLC-DAD 분석을 통해 15종의 페놀산과 2종의 플라보놀을 정량 분석하여 첨가 수준에 따른 기능성 성분의 변화를 규명하고자 하였다.
II. 연구방법
1. 재료
본 연구에 사용된 쌀가루는 국내산 백미를 100 mesh 체를 통과시킨 분말로, 건우상사(Cheomdan, Gwangju)에서 구입하였다. 감귤껍질 분말(100% Jeju)은 (주)맑은들(Hongcheon, Korea) 제품을 사용하였다. 부재료로는 전란액(Moguchon, Seoul, Korea), 우유(Maeil Dairies, Seoul, Korea), 설탕(CheilJedang, Seoul, Korea), 소금(Haepyo, Seoul, Korea), 버터(Seoulmilk, Yangju, Korea), 인스턴트 드라이이스트(Saf-instant, Lesaffre, France)를 사용하였다. 항산화능 및 페놀 화합물 분석에 사용된 시약은 Sigma-Aldrich(Burlington, MA, USA)로부터 구입하였다. HPLC 분석에 사용된 phenolic acid 및 flavonol 표준물질 17종도 Sigma-Aldrich(Burlington, MA, USA) 제품을 사용하였으며, 이동상은 HPLC 등급의 용매와 증류수를 사용하였다.
2. 감귤분말 첨가 쌀 모닝빵 제조법
감귤분말 첨가 쌀 모닝빵은 다음의 공정으로 제조하였다. 쌀가루(520 g), 우유(260 g), 계란(110 g), 설탕(90 g), 소금(8 g), 버터(70 g), 이스트(8 g)를 사용하였으며, 감귤껍질 분말은 쌀가루 대비 0, 3, 6, 9% 수준으로 첨가하였다. 반죽기(Founter, VFM10A, China)에 쌀가루, 설탕 소금, 이스트를 혼합하고 계란, 우유를 첨가하여 2분간 1단(저속)으로 13분간 반죽하였다. 반죽 후 발효기(Rakom. RJDNP-40-2-2, Korea) 온도 약 32℃, 상대습도(RH) 60% 조건에서 50분간 1차 발효 후, 40 g씩 분할하여 둥근 형태로 성형하고 발효기에서 추가로 60분간 발효하였다. 이후 오븐(Softmill, DHO2-33, Korea) 위불 175℃, 아래불 180℃로 15분간 구운 후 실온에서 충분히 냉각시켜 시료로 사용하였다.
3. 항산화능 분석
감귤분말 첨가 쌀 모닝빵의 항산화 활성을 평가하기 위하여 시료는 80% 에탄올을 사용하여 추출하였다. 동결 건조한 시료 1 g에 80% 에탄올 10 mL를 가한 후, 실온에서 1시간 진탕 추출하였고, 이를 3,000 rpm에서 20분간 원심 분리하여 상등액을 회수하였다. 회수한 추출액은 0.45 μm membrane filter로 여과 후 항산화능 분석에 사용하였으며, 분석 항목은 DPPH, ABTS, FRAP, 총 페놀 화합물, 총 플라보노이드 함량으로 구성하였다. 각 항목의 흡광도는 24-well plate를 사용하여 microplate reader(Infinite®200 Pro, NanoQuant, Tecan, Mannedorf, Switzerland)로 측정하였다.
DPPH(2,2-diphenyl-1-picrylhydrazyl) 라디칼 소거능은 Brand-Williams et al.(1995)의 방법에 따라 측정하였다. DPPH(0.1 mM) 용액을 100% 메탄올에 용해한 후 암실에서 30분간 안정화시켰다. 시료 추출액 100 μL에 DPPH 용액 900 μL를 혼합하여 실온 암실에서 30분간 반응시킨 후 517 nm에서 흡광도를 측정하였다. 대조구는 시료 대신 methanol을 사용하였으며, 항산화능은 Trolox를 기준물질로 하여 작성한 표준곡선을 이용하여 μmol Trolox equivalents (TE)/g sample로 환산하였다.
ABTS라디칼 소거능은 Re et al.(1999)의 방법을 일부 변형하여 측정하였다. ABTS(7 mM) 용액과 2.45 mM potassium persulfate 용액을 1:1 비율로 혼합하여 암실에서 16시간 반응시켜 ABTS+ 라디칼을 형성시킨 후, 흡광도 0.70 ± 0.020가 되도록 인산 완충용액(pH 7.4)을 희석하여 사용하였다. 시료 추출액 100 μL와 ABTS+ 용액 900 μL를 혼합한 후 실온에서 6분간 암실에서 반응시키고, 734 nm에서 흡광도를 측정하였다. Trolox를 기준물질로 한 표준곡선을 작성하여 μmol TE/g sample로 결과를 나타내었다.
FRAP 분석은 Benzie와 Strain(1996)의 방법을 따라 수행하였다. FRAP 시약은 300 mM acetate buffer(pH 3.6), 10 mM TPTZ(2,4,6-tripyridyl-s-triazine) in 40 mM HCl, 20 mM FeCl3ㆍ6H2O 용액을 10:1:1 비율로 혼합하여 제조하였다. 시료 추출액 100 μL에 FRAP 시약 900 μL를 첨가하여 37℃에서 30분간 반응시킨 후 593 nm에서 흡광도를 측정하였다. 항산화능은 Trolox 표준물질을 이용한 표준곡선으로부터 μmol TE/g sample로 환산하였다.
4. 총 페놀 화합물 함량 분석
총 페놀 화합물은 Singleton과 Rossi(1965)의 방법에 따라 측정하였다. 시료 추출액 100 μL에 Folin-Ciocalteu 시약 500 μL를 첨가하여 실온에서 5분간 반응시킨 후, 7.5% Na2CO3 용액 400 μL를 추가하고 암실에서 30분간 반응시켰다. 반응 후 725 nm에서 흡광도를 측정하였으며, gallic acid를 기준물질로 사용하여 작성한 표준곡선을 바탕으로 총 페놀 함량을 mg gallic acid equivalents (GAE)/g sample로 환산하였다.
5. 총 플라보노이드 함량 분석
총 플라보노이드 함량은 Chang et al.(2002)의 방법에 따라 측정하였다. 시료 추출액 500 μL에 5% NaNO2 용액 30 μL를 첨가하여 5분간 반응시킨 후, 10% AlCl3ㆍ6H2O 용액 30 μL를 첨가하여 6분간 반응시켰다. 이어서 1 M NaOH 200 μL를 첨가하여 총 1 mL로 만든 후 510 nm에서 흡광도를 측정하였다. Quercetin을 표준물질로 사용하였고, 총 플라보노이드는 mg quercetin equivalents(QE)/g sample로 나타내었다.
6. 총 카로티노이드 함량 분석
총 카로티노이드 함량은 Rodriguez-Amaya와 Kimura(2004)의 방법을 참고하여 분석하였다. 시료 1 g에 hexane:acetone:ethanol (2:1:1, v/v/v) 혼합용매 10 mL를 가하여 진탕 추출한 후 상층액을 분리하여 여과하였다. 여과액을 이용해 450 nm에서 흡광도를 측정하였고, β-carotene을 표준물질로 하여 μg β-carotene equivalents (BCE)/g sample로 계산하였다.
7. Phenolic acids 분석
유리형(free) phenolic acid는 Ainsworth와 Gillespie(2007)의 방법을 일부 변형하여 추출하였다. 동결 건조한 쌀 모닝빵 시료 5 g에 80% 메탄올 80 mL를 가한 후, 실온에서 1시간 동안 진탕 추출하였다. 동일한 과정을 총 3회 반복 수행하였으며, 각 회차마다 원심분리(3,000 rpm, 20분) 후 상등액을 회수하였다. 회수된 상등액은 모두 합한 뒤 Whatman No. 1 여과지로 여과하고, 감압 농축기(rotary evaporator)를 이용하여 40℃ 이하에서 용매를 제거하였다. 최종 잔류물은 메탄올 5 mL로 재용해한 후, 분석기기의 검출 범위에 적합하도록 적정 비율로 희석하여 0.22 μm membrane filter로 여과한 후 HPLC 분석에 사용하였다.
Phenolic acid 정량을 위한 HPLC 분석은 Shimadzu LC-20AD pump, CTO-20AC column oven, SIL-20AC auto-sampler, SPD-M20A 다이오드어레이 검출기(DAD), CBM-20A 시스템 컨트롤러 및 LC Workstation 소프트웨어(Shimadzu Corporation, Kyoto, Japan)로 구성된 시스템을 사용하였다. 분석 컬럼은 Phenomenex C18(2) 컬럼(150 × 3.0 mm, 3 μm, Phenomenex, Torrance, CA, USA)을 사용하였으며, LC-C18 guard column(4.0 × 10.0 mm)을 연결하였다. 이동상은 methanol과 증류수로 구성된 기울기 용매를 사용하였으며, 초기에는 methanol:H2O = 15:85 (v/v)로 시작하여, 40분 후에는 60:40 (v/v)까지 증가시키는 조건으로 설정하였다. 유속은 0.34 mL/min으로 유지하였고, 컬럼온도는 30℃, 주입량은 5 μL로 하였다. 검출은 220~550 nm의 파장에서 흡광도를 수집하였으며, 총 분석 시간은 90분이었다.
분석법의 신뢰성 확보를 위해 페놀산ㆍ플라보놀에 대해 검량선, 검출한계(LOD), 정량한계(LOQ), 회수율을 검증하였다. 표준용액(0.4∼32 mg/L)을 최소 5점 주입해 r²≥0.997의 검량선을 확립하였다. LOD와 LOQ는 신호 표준편차(σ)와 기울기(a)를 이용해 각각 3.3σ/a, 10σ/a로 계산했다. 회수율은 시료에 표준물을 첨가한 뒤 동일 전처리를 거쳐 회수율(%) = (첨가 후 농도 – 무첨가 농도)/첨가량 × 100으로 산출했으며, 모든 시험은 3회 반복하였다.
8. 통계분석
본 연구의 통계분석은 SPSS 통계 소프트웨어(Statistical Package for the Social Sciences, Version 29.0, SPSS Inc., Chicago, IL, USA)를 사용하여 수행하였으며, 각 측정값은 평균과 표준편차로 나타내었다. 시료 간 유의성 검정을 위해 일원분산분석(one-way ANOVA)을 실시한 후, 유의수준 p<0.05에서 Duncan의 다중범위검정(Duncan’s multiple range test)을 통해 시료 간의 유의성을 검정하였다.
III. 결과 및 고찰
1. 항산화능
감귤껍질 분말을 0%(대조군), 3%, 6%, 9% 수준으로 첨가한 쌀 모닝빵의 DPPH, ABTS, FRAP 항산화능을 비교한 결과는 Table 1과 같다. 감귤껍질 분말의 첨가량이 증가함에 따라 모든 항산화능 지표에서 유의한 증가(p<0.05)를 나타내었다.

Antioxidant activities (DPPH, ABTS, and FRAP) of morning bread supplemented with different levels of citrus peel powder (Citrus unshiu Marcov.)(μmol TE/g)
대조군의 DPPH 라디칼 소거능은 1.83 ± 0.07 μmol TE/g으로 가장 낮았으며, 9%는 7.37 ± 0.06 μmol TE/g으로 유의하게 높게 나타났다. ABTS 라디칼 소거능 역시 대조군(1.32 ± 0.08 μmol TE/g) 대비 9%(6.77 ± 0.03 μmol TE/g)에서 약 5배 이상 증가하였다. FRAP 환원력도 대조군의 3.33 ± 0.24 μmol TE/g에 비해 9%에서 14.55 ± 0.19 μmol TE/g으로 4배 이상 높았다.
이러한 결과는 감귤껍질 분말에 풍부하게 함유된 플라보노이드(hesperidin, narirutin 등) 및 페놀산류(ferulic acid, p-coumaric acid 등)와 같은 항산화 성분의 기여에 따른 것으로 해석된다(Li et al. 2006; González-Molina et al. 2010).
페놀성 화합물은 자유라디칼을 소거하거나 금속이온 킬레이션, 전자공여 등의 메커니즘을 통해 항산화 활성을 나타내는 것으로 잘 알려져 있다(Rice-Evans et al. 1997; Shahidi & Ambigaipalan 2015). 기능성 물질을 첨가한 유사 연구에서도 본 연구와 유사한 경향이 보고된 바 있다. Ceylan et al.(2021)은 돼지감자 분말과 저항성 전분을 함께 첨가한 기능성 케이크에서 총 페놀 함량과 ABTS 라디칼 소거능이 유의적으로 증가하였음을 보고하였으며, 또한 Wang et al.(2023)은 민들레(Taraxacum mongolicum)에서 추출한 플라보노이드 화합물을 이용한 가공 식품에서 DPPH 및 ABTS 항산화능이 현저히 개선되었음을 확인하였다. 이러한 결과는 식물성 소재의 첨가가 페놀산 함량을 높임으로써 제빵 제품의 항산화 기능성을 강화할 수 있음을 뒷받침한다.
2. 총 플라보노이드 및 총 카로티노이드 함량
감귤껍질 분말을 0%, 3%, 6%, 9% 첨가한 쌀모닝빵의 총 플라보노이드 함량(μmol QE/g) 및 총 카로티노이드 함량(μmol BCE/g)은 Fig. 1에 나타내었다. 감귤류는 플라보노이드 및 카로티노이드 함량이 높은 과일로, 이들 성분은 항산화 활성을 부여하는 기능성 소재로 활용되고 있다. 특히 가공식품에 감귤 껍질 유래 성분을 첨가할 경우 생리활성 물질의 함량 증가와 항산화능 향상에 기여할 수 있는 것으로 보고되고 있으며(Hollman & Katan 1999; Krinsky & Johnson 2005), González-Molina et al.(2010)은 감귤류 주스에 감귤껍질 추출물을 첨가하였을 때 총 플라보노이드 함량이 약 2배 증가하고, DPPH 소거능도 유의하게 향상되었다고 보고하였다.
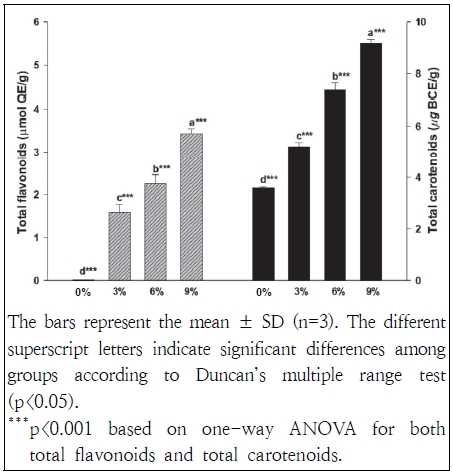
Total flavonoid (μmol QE/g, left axis) and total carotenoid (μmol BCE/g, right axis) contents in rice morning bread supplemented with 0, 3, 6, and 9% citrus peel powder.
총 플라보노이드 함량은 대조군에서 0.98 ± 0.05 μmol QE/g으로 가장 낮았고, 3%는 2.34 ± 0.09, 6%는 3.68 ± 0.11, 9%는 4.85 ± 0.12 μmol QE/g으로, 감귤껍질 분말 첨가량이 증가함에 따라 유의하게 증가하는 경향을 보였다(p<0.05). 총 카로티노이드 함량도 대조군에서 3.68 ± 0.21 μmol BCE/g으로 가장 낮았고, 9%에서는 9.48 ± 0.14 μmol BCE/g으로 측정되어, 대조군 대비 약 2.6배 증가하였다. 이는 감귤껍질 분말이 기능성 항산화 성분의 효과적인 공급원으로 작용하였음을 시사한다.
감귤껍질에는 hesperidin, narirutin, naringin과 같은 flavanone계 플라보노이드가 풍부하게 함유되어 있으며, 특히 hesperidin은 항산화, 항염증, 모세혈관 강화 등의 생리활성이 입증된 바 있다(González-Molina et al. 2010). 또한 감귤류에 존재하는 카로티노이드인 β-cryptoxanthin과 lutein, β-carotene은 지용성 항산화제이며, 체내에서 비타민 A로 전환되어 면역 기능, 시력 유지 등에도 중요한 역할을 한다(Johnson 2002; Rao & Rao 2007). 감귤껍질은 특히 이러한 성분이 과육보다도 더 고농도로 축적되어 있는 부분으로, 식품 부산물 중 기능성 원료로의 가치가 높다.
기능성 첨가물의 제빵 적용과 관련된 선행연구에서 Lee(2015)는 브로콜리 분말을 첨가한 흰빵에서 플라보노이드 함량 증가 및 항산화 활성이 유의하게 향상되었음을 밝혔고, Bing & Chun(2015)은 머루 분말이 첨가된 쌀 쉬폰케이크에서 총 폴리페놀 및 플라보노이드 함량 증가와 함께 DPPH 및 ABTS 라디칼 소거능이 향상되었다고 보고하였다.
3. 총 페놀 화합물 함량
Fig. 2는 감귤껍질 분말을 0%, 3%, 6%, 9% 수준으로 첨가한 쌀모닝빵의 총 페놀 함량(total phenolic content, TPC, μmol GAE/g)을 나타낸 결과이다. 감귤껍질 분말의 첨가 수준이 증가함에 따라 TPC 수치가 유의하게 증가하였으며, Duncan’s 다중 범위 검정 결과 처리구 간 유의한 차이가 확인되었다(p<0.05).
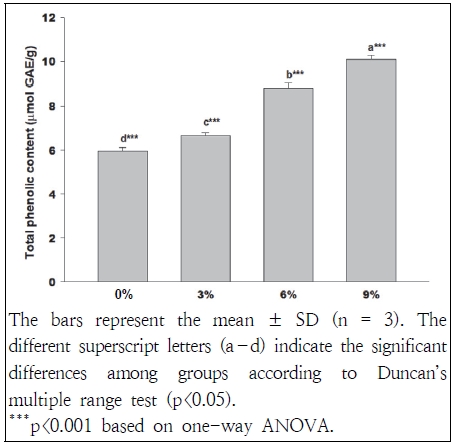
Total phenolic content (μmol GAE/g) in rice morning bread supplemented with 0, 3, 6, and 9% citrus peel powder (Citrus unshiu Marcov.).
대조군의 총 페놀 함량은 5.96 ± 0.16 μmol GAE/g으로 가장 낮았으며, 3%, 6%, 9%는 각각 6.67 ± 0.13, 8.83 ± 0.20, 10.11 ± 0.18 μmol GAE/g으로 나타났다. 특히 9%는 대조군 대비 약 69% 높은 수치를 보였으며, 이는 감귤껍질 분말이 쌀모닝빵의 페놀 화합물 함량을 효과적으로 증가시킨 것을 의미한다.
페놀 화합물은 식물에서 생성되는 2차 대사산물로, 일반적으로 항산화 작용, 항염증, 항암, 항균 활성을 포함한 다양한 생리활성을 나타낸다(Pandey & Rizvi 2009). 이러한 기능성은 페놀 화합물이 갖는 전자공여 능력과 금속 킬레이션 작용, 라디칼 소거능 등에 기인하며, 이는 식품 내 산패 억제 및 인체의 산화적 스트레스를 저감시키는 데 기여한다(Rice-Evans et al. 1997).
감귤껍질은 특히 flavonoids 계열과 함께 hydroxycinnamic acid, caffeic acid, p-coumaric acid, ferulic acid 등의 다양한 phenolic acid를 다량 함유하고 있으며, 이들은 항산화 활성이 뛰어난 것으로 보고되어 있다(Li et al. 2006; González-Molina et al. 2010). 감귤의 주요 페놀 성분 중 하나인 hesperidin은 높은 수용성과 안정성을 가지고 있어 제빵과 같은 고온 공정에도 적용 가능성이 높다는 장점이 있다.
최근 기능성 식품 개발에 있어 식물 유래 소재의 항산화 성분을 활용한 제과 제품 연구가 활발히 진행되고 있다. 특히 돼지감자(Jerusalem artichoke)는 이눌린을 비롯한 프리바이오틱 섬유소와 항산화 물질이 풍부한 식재료로 주목받고 있다. Ceylan et al.(2021)은 돼지감자 분말과 저항성 전분을 활용한 케이크 제형에서 총 페놀 함량 및 ABTS 라디칼 소거능이 유의적으로 향상됨을 보고하였으며, 이는 식물성 분말 소재가 항산화 활성을 증대시킬 수 있는 유효한 배합임을 시사한다.
또한 민들레(Taraxacum officinale)는 플라보노이드와 페놀산이 풍부한 대표적인 기능성 식물로, 다양한 가공식품에 적용되고 있다. Elcik과 Kirkin(2024)은 민들레 뿌리 추출물을 활용한 주입 음료에서 콜드 플라즈마 전처리 시 총 폴리페놀 함량 및 DPPH/ABTS 항산화 활성의 유의한 증가를 확인하였고, 이는 추출 조건과 가공 방식이 식물성 소재의 기능성 증진에 큰 영향을 미칠 수 있음을 보여준다.
본 연구에서 감귤껍질 분말을 쌀 모닝빵 반죽에 첨가하였을 때, 첨가 수준이 증가함에 따라 총 페놀산 및 플라보노이드 함량이 증가하고, 이에 따른 항산화능(DPPH, ABTS, FRAP) 또한 유의하게 향상되었다. 이는 감귤 껍질이 항산화 활성을 갖는 식물성 분말로서 제빵 제품에 적용 가능한 기능성 소재임을 의미하며, 선행연구들과 같이 기능성과 품질 개선을 동시에 도모할 수 있는 가능성을 제시한다.
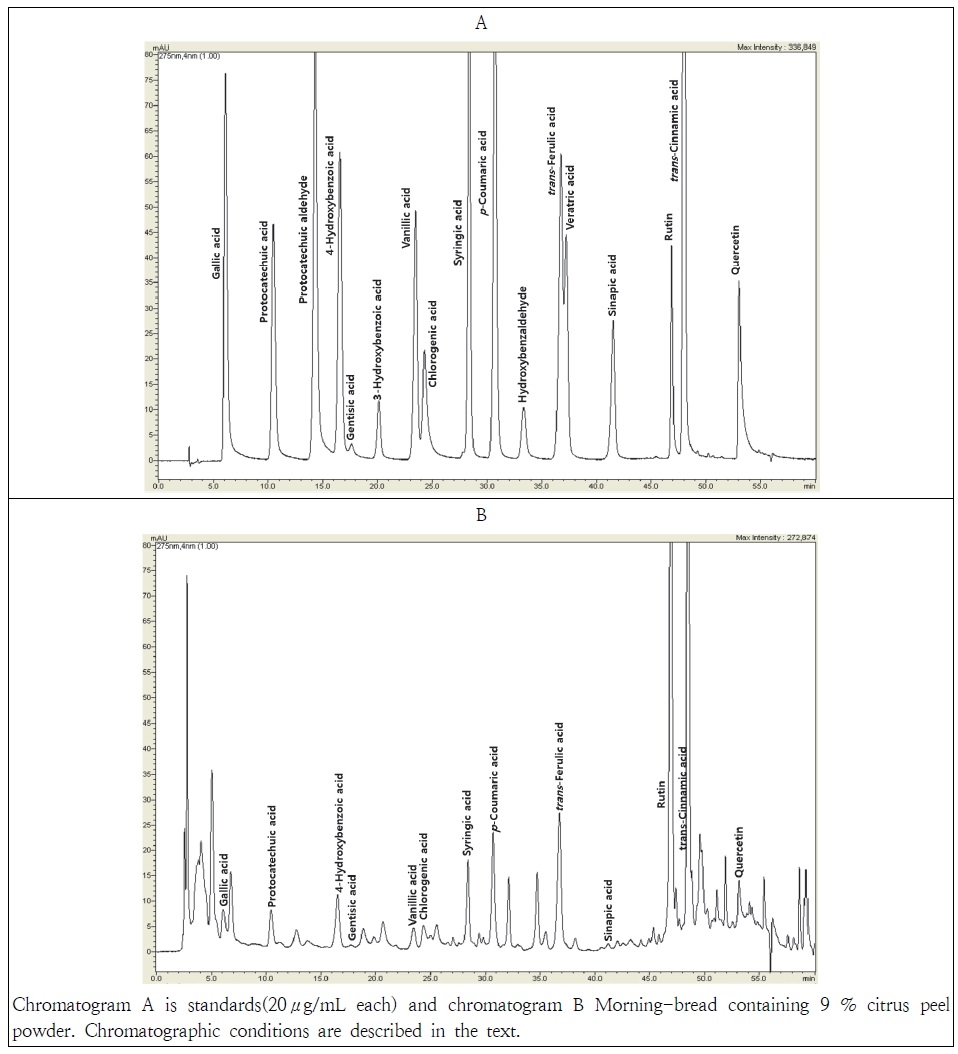
4. HPLC-DAD를 이용한 페놀산 및 플라보놀의 정량 특성
HPLC-DAD를 이용하여 페놀산 및 플라보놀 화합물의 정량 분석을 위한 크로마토그램(Fig. 3)과 선형성(linearity), 검출한계(LOD), 정량한계(LOQ), 회수율(recovery) 및 상관계수(r2) 등 분석법의 검증 지표를 Table 2에 나타내었다. 총 15종의 페놀산과 2종의 플라보놀(Rutin, Quercetin hydrate)을 대상으로 하였으며, 표준용액의 농도 범위는 0.4∼32.0 mg/L 범위에서 설정되었다.

Linearity, sensitivity, and recovery parameters for phenolic acids and flavonols quantified by HPLC-DAD
모든 화합물의 상관계수(r2)는 0.9973 이상으로, 정량법의 우수한 직선성을 확보하였음을 확인할 수 있었다. 특히 Gallic acid, p-Coumaric acid, Chlorogenic acid, Rutin 등의 r2 값은 0.9999로 나타나 매우 높은 정량 신뢰도를 보였다. 이는 분석기기와 조건이 정량에 적합하게 설정되었으며, 다양한 페놀계 화합물에 대해 정밀한 분석이 가능함을 의미한다(ICH Q2(R1) 2005).
검출한계(LOD)는 0.08∼0.24 mg/L, 정량한계(LOQ)는 0.24∼0.76 mg/L의 범위를 보였으며, 이는 미량 성분 분석에 적합한 민감도를 지니고 있음을 시사한다. 대부분의 화합물에서 LOD가 0.1 mg/L 이하로 설정되어, 감귤껍질 등 식물성 소재의 미량 페놀 성분 분석에 활용하기에 충분한 감도를 갖춘 것으로 평가된다.
회수율은 87.7∼99.8% 범위로 나타났으며, 이는 AOAC 기준(80∼110%)을 충족하거나 초과하는 값으로, 본 분석법의 정확성과 신뢰성을 뒷받침해준다(AOAC 2000). 특히 3-Hydroxybenzoic acid(99.79%), Rutin(97.82%), trans-Cinnamic acid(97.66%) 등의 회수율은 매우 우수한 수준이었다. 이는 매트릭스 간섭(matrix effect)이 최소화되었기 때문으로 판단된다.
페놀산과 플라보놀은 항산화 활성을 유도하는 주요 기능성 성분으로, 그 구조적 특성에 따라 라디칼 소거능, 금속 이온 킬레이션, 과산화 억제 등 다양한 메커니즘을 통해 작용한다(Rice-Evans et al. 1997; Manach et al. 2004). 특히 감귤껍질에는 hesperidin, naringin, rutin 등의 플라보노이드와 ferulic acid, caffeic acid, gallic acid 등의 페놀산이 혼재되어 있으며, 이들의 복합적 작용이 항산화 효과를 증폭시킨다(González-Molina et al. 2010).
5. 감귤껍질 분말 첨가 쌀모닝빵의 페놀산 및 플라보놀 함량
Table 3은 감귤껍질 분말을 0%, 3%, 6%, 9% 수준으로 첨가한 쌀모닝빵 내 개별 페놀산(μg/g) 및 플라보놀 성분의 함량을 나타낸 것이다. 총 14종의 페놀산과 2종의 플라보놀을 분석하였으며, 감귤껍질 분말의 첨가 수준이 증가할수록 대부분의 성분에서 유의한 증가(p<0.05)가 관찰되었다.

Contents of phenolic acids and flavonols (µg/g dry weight) in morning bread supplemented with citrus peel powder (Citrus unshiu Marcov.) at 3%, 6%, and 9%
대조군에서는 3-hydroxybenzoic acid, protocatechuic aldehyde, gentisic acid, hydroxybenzaldehyde, veratric acid, Rutin, quercetin hydrate 등이 검출되지 않았으며, 이는 감귤껍질이 해당 성분의 주된 공급원임을 의미한다. 특히 9%에서 syringic acid(23.31 ± 0.47 μg/g), trans-Ferulic acid(48.69 ± 1.11 μg/g), vanillic acid(16.70 ± 0.50 μg/g), chlorogenic acid(2.05 ± 0.03 μg/g) 등 다양한 페놀산의 함량이 대조군 대비 유의하게 높게 나타났다.
플라보놀의 경우 대조군에서는 검출되지 않았으나, 3% 이상부터 rutin과 quercetin hydrate가 모두 정량되었으며, 9%에서 각각 3.26 ± 0.08 μg/g, 12.15 ± 0.29 μg/g으로 가장 높은 값을 나타냈다. 총 플라보놀 함량은 대조군의 0.00 μg/g에서 9%의 15.41 μg/g으로 증가하였다.
감귤껍질에는 항산화, 항염증, 항균 활성을 지닌 다양한 생리활성 물질이 함유되어 있으며, 이 중에서도 페놀산과 플라보놀은 주요한 기능성 성분으로 작용한다(Rice-Evans et al. 1997; Manach et al. 2004). 특히 hesperidin, naringin, rutin 등 감귤류 특유의 플라보노이드는 생리활성이 우수할 뿐 아니라, 제빵과 같은 고온의 가공 조건에서도 비교적 안정하게 유지되는 특성이 있다(González-Molina et al. 2010). 본 연구에서 syringic acid, ferulic acid, p-coumaric acid, chlorogenic acid 등의 페놀산 함량이 증가한 것은 이러한 감귤껍질 유래 성분이 실제 제품 내에서 기능적으로 반영된 결과로 볼 수 있다.
또한, 총 페놀산 함량은 대조군(66.16 μg/g)에 비해 9%(129.04 μg/g)는 약 2배 이상 증가하였으며, 이는 앞서 제시된 총 페놀 함량 및 항산화능 증가 경향(Table 1, Fig. 2)과 일치한다. 이는 페놀산 성분이 실질적으로 항산화 기여 성분임을 입증하는 결과이다.
유사한 경향은 선행 연구들에서도 확인된 바 있다. Ceylan et al.(2021)은 돼지감자 분말과 저항성 전분을 첨가한 기능성 케이크에서 chlorogenic acid, ferulic acid 등 주요 페놀산의 함량이 유의적으로 증가하고, ABTS 라디칼 소거능 또한 향상되었다고 보고하였다. 이와 유사하게, Elcik & Kirkin(2024)은 민들레 뿌리 추출물을 활용한 주입액에서 콜드 플라즈마 전처리를 통해 총 폴리페놀 함량과 DPPH 및 ABTS 항산화 활성 간의 밀접한 상관관계를 밝혀낸 바 있다. 이러한 결과들은 식물성 분말 소재가 항산화성분의 증가뿐만 아니라 항산화 활성을 실질적으로 강화할 수 있는 수단임을 시사하며, 본 연구에서 감귤 껍질 분말 첨가에 따른 페놀 화합물 함량 증가와 항산화능 향상 결과를 지지한다.
6. 항산화지표 간의 상관관계 분석
감귤껍질 분말이 첨가된 쌀모닝빵의 항산화 관련 지표 간의 Pearson 상관계수(r)와 two-tailed 검정 p-value를 분석한 결과를 Table 4에 나타냈다. 항산화 지표로는 총 페놀 함량, 총 플라보노이드, 총 카로티노이드 함량, DPPH, ABTS, FRAP이 포함되었다.

Pearson correlation coefficients (r)1) and two-tailed p-values2) among the antioxidant indices of rice morning bread fortified with citrus powder
총 페놀 함량은 DPPH (r=0.997, p=0.003), ABTS (r=0.997, p=0.003), FRAP (r=0.998, p=0.002)와 매우 높은 양의 상관관계를 보여 통계적으로 유의하였다(p<0.05). 이는 총 페놀 화합물이 항산화능의 주요 기여 성분임을 시사한다. 또한 총 페놀 함량은 총 플라보노이드(r=0.970, p=0.030), 총 카로티노이드(r=0.992, p=0.008)와도 높은 상관성을 보여, 플라보노이드 및 카로티노이드 성분 역시 항산화능에 기여함을 확인할 수 있다.
DPPH와 ABTS는 완전한 상관(r=1.000, p<0.001)을 보였으며, FRAP과도 r=0.991(p= 0.009)로 유의한 상관성을 나타냈다. 이는 세 가지 항산화능 지표가 서로 유사한 메커니즘을 통해 작용하며, 감귤껍질 분말 함량 변화에 따라 일관된 반응을 보였다. 이러한 경향은 항산화 평가 지표 간 상호 보완성과 신뢰성을 높여준다(Rice-Evans et al. 1997).
총 플라보노이드와 총 카로티노이드 함량은 FRAP과 각각 r=0.979(p=0.021), r=0.993(p=0.007)로 매우 높은 유의한 상관관계를 보였다. 이는 플라보노이드 및 카로티노이드가 전자공여 혹은 금속이온 환원 능력 측면에서 항산화 활성을 나타낼 수 있음을 뒷받침하는 결과이다(Krinsky & Johnson 2005).
7. 개별 페놀산과 항산화 활성 간의 상관관계 분석
Table 5는 감귤껍질 분말을 첨가한 쌀모닝빵에서 정량된 개별 페놀산 함량과 항산화 활성 지표(DPPH, ABTS, FRAP) 간의 Pearson 상관계수(r) 및 two-tailed 검정 p 값을 제시한 것이다. 분석 결과, 모든 페놀산이 세 가지 항산화 지표와 높은 양의 상관관계를 나타내었으며, 대부분 통계적으로 유의한 수준(p<0.05)이었다. 본 연구에서는 개별 페놀산과 항산화 활성 지표 간의 상관관계를 정밀하게 분석하기 위해, HPLC-DAD로 정량된 12종의 주요 phenolic acid를 기준으로 상관분석을 수행하였다.

Pearson correlation coefficients (r)1) and p-values2) between individual phenolic acid contents and antioxidant activities (DPPH, ABTS, FRAP) of rice morning bread fortified with citrus powder
반면, total flavonoids와 total carotenoids는 각각 AlCl₃ 착화합 반응과 β-carotene 기반 흡광도 측정에 따라 비특이적 정량법(spectrophotometric total content)으로 측정된 지표로, 해당 측정값은 특정 단일 화합물이 아닌 혼합물의 총량을 나타낸다. 따라서 개별 페놀산과 직접적으로 비교 가능한 구조적 특이성이 부족하며, 통계적으로 독립된 항목으로 분석하는 것이 적절하지 않다고 판단하였다. 또한 total flavonoids 및 carotenoids는 이미 앞선 Table 4에서 총 페놀, 항산화 지표들과의 상관관계가 유의하게 확인되었기 때문에, Table 5에서는 개별 페놀산과 항산화 활성 간의 직접적 기여도를 해석하는 데에 초점을 맞추기 위해 제외하였다.
DPPH 라디칼 소거능과의 상관계수는 protocatechuic acid(r=0.981, p=0.019), 4-hydroxybenzoic acid(r=0.979, p=0.021), syringic acid(r=0.979, p=0.021) 등 다수의 페놀산에서 0.97이상으로 나타나, 페놀산이 DPPH 소거능에 기여하는 주요 항산화 성분임을 시사한다. ABTS와의 상관계수도 전반적으로 유사한 양상을 보였으며, protocatechuic acid(r=0.980, p=0.020), vanillic acid(r=0.978, p=0.023), trans-ferulic acid(r=0.978, p=0.023) 등이 높게 나타났다.
FRAP(환원력 지수)의 경우에도 대부분의 페놀산이 0.95 이상으로 높은 상관성을 나타냈으며, protocatechuic acid(r=0.961), chlorogenic acid(r=0.956), syringic acid(r=0.956) 등에서 유의한 관계가 확인되었다. 다만, 일부 성분(Gentisic acid, trans-Cinnamic acid)은 FRAP에서만 유의수준 p<0.05를 만족하지 못했으며, 이는 측정 민감도나 함량의 미세한 차이에 기인한 것으로 해석된다.
총 페놀 함량은 세 항산화 지표 모두와 매우 높은 상관관계를 나타냈으며, DPPH(r=0.979, p=0.021), ABTS(r=0.977, p=0.023), FRAP(r=0.956, p=0.044)로 각각 통계적으로 유의하였다. 이는 개별 페놀산의 총합이 곧 항산화 활성에 크게 기여함을 의미하며, 쌀모닝빵의 항산화 기능성 향상에 감귤껍질 유래 페놀화합물이 중요한 역할을 하고 있음을 보여준다(Rice-Evans et al. 1997; Manach et al. 2004).
이러한 경향은 선행 연구와도 일치하며, 여러 연구에서 특정 페놀산 성분(예: ferulic acid, gallic acid, vanillic acid 등)이 DPPH, ABTS 라디칼 소거 및 FRAP 활성과 높은 상관관계를 갖는 것으로 보고된 바 있다(Shahidi & Ambigaipalan 2015). 특히 감귤류는 naringin, hesperidin과 같은 플라보노이드뿐 아니라 다양한 페놀산을 함유하고 있어 복합적 항산화 기작이 작용하는 것으로 추정된다(González-Molina et al. 2010).
IV. 요약 및 결론
본 연구는 쌀가루의 0, 3, 6, 9%를 감귤껍질 분말로 대체하여 글루텐-프리 모닝빵을 제조한 후 페놀 화합물 조성 및 항산화 활성을 측정하였다. 완제품의 총 페놀 함량, 개별 phenolic acids(15종), 총 플라보노이드ㆍ카로티노이드 함량을 분석하였으며, DPPH, ABTS, FRAP법으로 항산화능을 평가하였다. 감귤껍질 분말을 첨가한 쌀 모닝빵은 첨가량이 증가할수록 총 페놀, 플라보노이드, 카로티노이드 함량이 유의적으로 증가하였으며, 이와 함께 DPPH, ABTS, FRAP 등 항산화 활성 지표 또한 뚜렷한 향상 양상을 보였다. 총 페놀 화합물 함량은 항산화능과 높은 양의 상관관계를 나타내어, 기능성 성분으로서 페놀 화합물이 항산화 기전에 핵심적으로 작용함을 확인할 수 있었다.
HPLC-DAD를 이용한 분석 결과, gallic acid, syringic acid, vanillic acid, chlorogenic acid 등 주요 페놀산이 감귤껍질 분말 첨가에 따라 유의하게 증가하였고, 3% 이상에서는 rutin과 quercetin hydrate 등 플라보놀도 검출되어 기능성 성분이 실제로 강화되었음을 확인하였다. 특히 개별 페놀산과 항산화 활성 간의 상관관계 분석에서 대부분의 성분이 r>0.97 수준의 높은 유의성을 보였다는 점은, 이들 화합물이 항산화 활성을 유도하는 주요한 생리활성 물질임을 뒷받침한다.
이는 감귤껍질 분말이 단순한 첨가재를 넘어서 항산화 기능성을 부여할 수 있는 유효한 천연 소재임을 입증한 것으로, 제과ㆍ제빵 산업에서의 기능성 강화 전략에 효과적으로 활용될 수 있음을 보여준다. 본 연구의 결과는 감귤껍질을 포함한 과일 껍질류 부산물의 고부가가치 식품소재화에 대한 과학적 근거를 제공함과 동시에, 글루텐 프리 베이커리의 품질 및 기능성 향상 전략 수립에 기여할 수 있을 것으로 기대된다.
References
-
Ainsworth EA, Gillespie KM(2007) Estimation of total phenolic content and other oxidation substrates in plant tissues using Folin-Ciocalteu reagent. Nat Protoc 2(4), 875-877.
[https://doi.org/10.1038/nprot.2007.102]

- AOAC(2000) Official Methods of Analysis of AOAC International. 17th ed. Rev 2. Association of Official Analytical Chemists, Gaithersburg, MD, USA
-
Benzie IFF, Strain JJ(1996) The ferric reducing ability of plasma (FRAP) as a measure of “antioxidant power”: the FRAP assay. Anal Biochem 239(1), 70-76.
[https://doi.org/10.1006/abio.1996.0292]

-
Bourekoua H, Benatallah L, Zidoune MN, Rosell CM(2016) Developing gluten free bakery improvers by hydrothermal treatment of rice and corn flours. LWT-Food Sci Technol 73, 342-350.
[https://doi.org/10.1016/j.lwt.2016.06.032]

-
Brand-Williams W, Cuvelier ME, Berset C(1995) Use of a free radical method to evaluate antioxidant activity. LWT-Food Sci Technol 28(1), 25-30.
[https://doi.org/10.1016/S0023-6438(95)80008-5]

-
Ceylan H, Bilgiçli N, Cankurtaran T(2021) Improvement of functional cake formulation using Jerusalem artichoke flour as inulin source and resistant starch (RS4). LWT- Food Sc Tech 145, 111301.
[https://doi.org/10.1016/j.lwt.2021.111301]

-
Chang CC, Yang MH, Wen HM, Chern JC(2002) Estimation of total flavonoid content in propolis by two complementary colorimetric methods. J Food Drug Anal 10(3), 178-182.
[https://doi.org/10.38212/2224-6614.2748]

-
Cornejo F, Rosell CM(2015) Physicochemical properties of long rice grain varieties in relation to gluten free bread quality. LWT-Food Sci Technol 62(2), 1203-1210.
[https://doi.org/10.1016/j.lwt.2015.01.050]

-
Elcik BE, Kirkin C(2024) Quality and antioxidant activity of dandelion root infusions as affected by cold plasma pretreatment. Food Sci Nutr 12(1), 526-533.
[https://doi.org/10.1002/fsn3.3791]

-
González-Molina E, Domínguez-Perles R, Moreno DA, García-Viguera C(2010) Natural bioactive compounds of citrus limon for food and health. J Pharm Biomed Anal 51(2), 327-345.
[https://doi.org/10.1016/j.jpba.2009.07.027]

-
Hollman PCH, Katan MB(1999) Dietary flavonoids: intake, health effects and bioavailability. Food Chem Toxicol 37(9-10), 937-942.
[https://doi.org/10.1016/S0278-6915(99)00079-4]

- ICH(International Council for Harmonisation)(2005) ICH harmonised tripartite guideline Q2(R1): Validation of analytical procedures: text and methodology. Geneva, Switzerland. Available from https://database.ich.org/sites/default/files/Q2%28R1%29%20Guideline.pdf, [cited 2025 July 3]
-
Johnson EJ(2002) The role of carotenoids in human health. Nutr Clin Care 5(2), 56-65.
[https://doi.org/10.1046/j.1523-5408.2002.00004.x]

-
Krinsky NI, Johnson EJ(2005) Carotenoid actions and their relation to health and disease. Mol Aspects Med 26(6), 459-516
[https://doi.org/10.1016/j.mam.2005.10.001]

-
Lee HN, Park TS, Yu OK, Byun MS, Cha YS(2016) Development of morning bread fortified citrus peels powders and its evaluation of biological activity by human trial. J Nutr Health 49(3), 144–152.
[https://doi.org/10.4163/jnh.2016.49.3.144]

-
Lee SH(2015) Quality and antioxidant properties of white breads enhanced with broccoli (Brassica oleracea L.) powder. Korean J Food Cook Sci 31(5), 614–622.
[https://doi.org/10.9724/kfcs.2015.31.5.614]

-
Lee SH, Park SH, Park H(2024) Assessing the feasibility of biorefineries for a sustainable citrus waste management in Korea. Molecules 29(7), 1589.
[https://doi.org/10.3390/molecules29071589]

-
Li BB, Smith B, Hossain MM(2006) Extraction of phenolics from citrus peels: II. Enzyme-assisted extraction method. Sep Purif Technol 48(2), 189-196.
[https://doi.org/10.1016/j.seppur.2005.07.019]

-
Li S, Lo CY, Ho CT(2006) Hydroxylated polymethoxyflavones and methylated flavonoids in sweet orange (Citrus sinensis) peel. J Agric Food Chem 54(12), 4176-4185
[https://doi.org/10.1021/jf060234n]

-
Manach C, Scalbert A, Morand C, Rémésy C, Jiménez L(2004) Polyphenols: food sources and bioavailability. Am J Clin Nutr 79(5), 727–747.
[https://doi.org/10.1093/ajcn/79.5.727]

-
Manthey JA, Grohmann K(2001) Phenols in citrus peel byproducts. Concentrations of hydroxycinnamates and polymethoxylated flavones in citrus peel molasses. J Agric Food Chem 49(7), 3268-3273.
[https://doi.org/10.1021/jf010011r]

-
Pandey KB, Rizvi SI(2009) Plant polyphenols as dietary antioxidants in human health and disease. Oxid Med Cell Longev 2(5), 270-278
[https://doi.org/10.4161/oxim.2.5.9498]

-
Park J, Kim HS(2023) Rice‑based gluten‑free foods and technologies: a review. Foods 12(22), 4110.
[https://doi.org/10.3390/foods12224110]

-
Rao AV, Rao LG(2007) Carotenoids and human health. Pharmacol Res 55(3), 207-216.
[https://doi.org/10.1016/j.phrs.2007.01.012]

-
Re R, Pellegrini N, Proteggente A, Pannala A, Yang M, Rice-Evans C(1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Radic Biol Med 26(9-10), 1231-1237.
[https://doi.org/10.1016/S0891-5849(98)00315-3]

-
Rice-Evans C, Miller N, Paganga G(1997) Antioxidant properties of phenolic compounds. Trends Plant Sci 2(4), 152–159.
[https://doi.org/10.1016/S1360-1385(97)01018-2]

- Rodriguez‑Amaya DB, Kimura M(2004) HarvestPlus handbook for carotenoid analysis (HarvestPlus Technical Monograph No. 2). Washington, DC & Cali: IFPRI & CIAT
- Rural Development Administration(2022) Korean Food Composition Table (9th rev.). National Institute of Agricultural Sciences, Jeonju, Korea. Available from https://koreanfood.rda.go.kr, . [cited 10 July 2025]
-
Sedej I, Sakač M, Mandić A, Mišan A, Tumbas V, Čanadanović-Brunet J, Šimurina O(2011) Quality assessment of gluten-free crackers based on buckwheat flour. LWT-Food Sci Technol 44(3), 694–699.
[https://doi.org/10.1016/j.lwt.2010.11.010]

-
Shahidi F, Ambigaipalan P(2015) Phenolics and polyphenolics in foods, beverages and spices: antioxidant activity and health effects – a review. J Functional Foods 18, 820–897. dio:10.1016/j.jff.2015.06.018
[https://doi.org/10.1016/j.jff.2015.06.018]

-
Singleton VL, Rossi JA(1965) Colorimetry of total phenolics with phosphomolybdic-phosphotungstic acid reagents. Am J Enol Vitic 16(3), 144-158.
[https://doi.org/10.5344/ajev.1965.16.3.144]

- Song JY, Shin M(2007) Effects of soaking and particle sizes on the properties of rice flour and gluten-free rice bread. Food Sci Biotechnol 16(5), 759–764
-
Wang R, Li W, Fang C, Zheng X, Liu C(2023) Extraction and identification of new flavonoid compounds in dandelion Taraxacum mongolicum with evaluation of antioxidant activities. Scientific Reports 13(1), 2166.
[https://doi.org/10.1038/s41598-023-28775-x]